编辑的话:去年,果壳网科学人报道了一篇发表在《自然》上的论文。撰写报道时,我采访了论文作者刘旭博士,他不但亲切详细地回答了所有采访问题,还仔细审阅了稿件并提出修改意见。临了刘旭对我说:“这次合作愉快,希望今后能有机会继续!”谁料,这样的机会,竟已永远消失。前不久,我收到复旦大学丁澦老师的邮件,才惊悉刘旭博士去世的消息。为了纪念英年早逝的同窗好友,丁澦写了以下文字:
一个月前,我的好友刘旭(Liu Xu)去世了。这个世界上最顶尖的记忆研究者之一,对小鼠记忆进行操纵的先驱科学家,最后却以一场猝不及防的病逝在亲朋好友中留下了一片难以忘却的伤感记忆。
 刘旭(1977.11.23-2015.2.8),美国西北大学神经生物学系助理教授。
刘旭(1977.11.23-2015.2.8),美国西北大学神经生物学系助理教授。
我认识刘旭已经19年了。七年同窗,刘旭那过人的天赋和过人的勤勉,至今仍历历在目。他1996年至1999年就读于复旦大学生命科学学院理科基地班,是我们班的小班长。刘旭用3年半的时间就完成本科学业,以优异成绩获学士学位,直升复旦大学生命科学学院遗传学系研读硕士。后来,他师从乔守怡教授,主要研究一系列人类新基因在果蝇中的克隆、表达和功能。
2002年至2008年,刘旭作为博士生在贝勒医学院(Baylor College of Medicine)分子与细胞生物学系罗纳德·戴维斯(Ronald L. Davis)教授实验室进行了果蝇记忆相关的研究,迈入了记忆研究领域。这期间,这位大学时同学眼中的“学神”在《自然·神经科学》等主流学术期刊发表了多篇论文。
随后,刘旭加入麻省理工大学(MIT)诺贝尔奖获得者利根川进教授的实验室,以小鼠为模型进行了记忆相关的研究,相关研究和评述发表在《自然》《科学》和《细胞》等顶级学术期刊。他们给小鼠移植虚假记忆的杰出工作还入选《科学》评选的2014年度全球十大科学突破。刘旭及其合作伙伴斯蒂夫·拉米雷斯(Steve Ramirez)因为操纵记忆的突破性工作获得2014年度美国史密森尼创造力大奖(Smithsonian American Ingenuity Award),并两次受邀在广为互联网科技迷所熟知的TED大会演讲。
短短几年间,刘旭就达成了在顶尖的“CNS”(Cell,Nature和Science)发文的成就。2015年起,刘旭被位于芝加哥的西北大学聘为神经生物学系助理教授。我和同学们都在憧憬着,在不远的将来,他将把他在MIT尚未完成的记忆研究深入推进,为推进人们对大脑的认知做出更杰出的贡献。
直到一个越洋电话,让这一切戛然而止。2月8日,刘旭在芝加哥寓所因突发疾病骤然离世。诺贝尔奖获得者利根川进在他追思会上说:“刘旭是标记和操纵记忆领域研究的第一人,他的贡献会永远留在人类的集体记忆中。”
我想,对他最好的纪念,也许就是将其突破性的科学贡献介绍给世人,使大家知道曾经有这么一位杰出的华人科学家,就这么低调地生活在他们身边,兢兢业业地做出了划时代的工作。
 刘旭及合作伙伴Steve Ramirez因为操纵记忆的开创性研究,获2014年度美国史密森尼创造力大奖。图片来源:Irvin Serrano/ smithsonianmag.com
刘旭及合作伙伴Steve Ramirez因为操纵记忆的开创性研究,获2014年度美国史密森尼创造力大奖。图片来源:Irvin Serrano/ smithsonianmag.com
海马与杏仁核,记忆之源
现在,小学生都能理解“人类依靠大脑进行学习和记忆”这一基本常识。但其实,直到1664年,英国牛津大学的托马斯·威利斯(Thomas Willis)才第一次明确指出是大脑而非心脏是思维的器官。随后的几个世纪,科学家们致力于将大脑各个区域的功能加以明确。比如在1920年代,美国著名心理学家卡尔·拉施里(Karl Lashley)提出,记忆的缺陷程度与脑损伤的具体部位无关,而只和损伤的大小有关,因此记忆不是储存在特定部位,而是弥散在大脑里的[1]。他的观点流行了很多年,直到1957年,斯克维尔(Scoville)与米尔纳(Milner)才在关于著名的癫痫病人亨利·莫莱森(Henry Molaison,即H.M.)的病例报告中提出新的观点:他们将长时程记忆定位到大脑的海马区,而不是拉施里所说的弥散分布[2]。H.M.因为车祸后遗症造成的严重癫痫,不得不在27岁时接受手术,吸除了大部分的海马组织。他术后出现非常严重且奇特的后遗症——尽管他具有完好的短期记忆,但因为海马受损,无法将短期记忆转变为长期记忆了,与此同时,他依然会做他在27岁前学会的事情,也记得他小时候的事情[3]。后来的各种研究结果提示,记忆很可能是存在于特定脑细胞中的,而这些细胞主要集中在脑中的小块区域:海马(Hippocampus)和杏仁核(Amygdala)。这已成为科学界的普遍共识。
然而,在面对如何精确定位这些特定脑细胞、改变细胞功能的问题时,科学家们却始终不得其法。在这个大背景下,刘旭和同事利用光遗传学(Optogenetics)方法,不仅巧妙地标记了与特定记忆相关的神经元,而且通过操纵神经元活动激活了以往的记忆,并进一步给小鼠移植了虚假记忆。后来,他们又把记忆定位到脑内更精确的区域,鉴定了海马和杏仁核在记忆过程中的各自独特作用。
对刘旭的开创性工作影响最大的,是对两种新技术的结合运用——一系列转基因小鼠品系的建立,以及光遗传学操纵技术的成熟。正是将这两种技术进行了巧妙的整合,刘旭得以标记特定的细胞并通过激光对这群负责特定记忆的细胞进行了操作。
食物+刺激,瞄准小鼠的“记忆细胞”
他们最终选定转入了光敏感通道的转基因小鼠,它们的某些特定基因可被四环素(Tet)或其结构类似物多西环素(Dox)所调控。通俗地说,他们相当于将光敏感通道的基因转到小鼠里,并且在前面放了两组“开关”。这两组“开关”串联,必须同时开放才可最终生产光敏感通道。
其中一组开关由多西环素所控制,只要给小鼠吃含有多西环素的鼠粮,对应的“开关”就处于关闭状态,光敏感通道不能被生产出来。相反,小鼠的食物中不含多西环素,这一组开关就打开了。第二组开关则负责控制具体在哪些神经元里面允许生产光敏感通道蛋白。
其他科学家前期的研究表明,在分子生物学层面,当形成新记忆的时候,涉及到一系列新蛋白质的合成,其中c-fos就是其中一个被激活的基因。每当受到新的刺激时,相应的神经元被激活后会在较短的时间内表达c-fos蛋白。刘旭等人把控制c-fos表达的启动子作为第二套“开关”加在了多西环素开关的前面。这样在转基因小鼠里,只有活跃的神经元才会在两组开关的共同作用下,产出光敏感通道蛋白。
如果将刘旭与他的同事比作射击运动员,那么这两重开关能确保他实现对特定活动目标的精确射击:多西环素控制的第一重开关相当于是枪的保险,非选择性地针对所有神经元,作为第二重开关的c-fos启动子则相当于扣动扳机前的瞄准过程,确保“射击者”能有的放矢,专一性地针对特定活跃的神经元进行射击。
假定两组开关都打开,目标神经元生产出的光敏感通道又有什么用呢?这就涉及到第二种突破性的技术,光遗传学。2010年,刘旭和利根川进在《细胞》上发表评述,详细介绍了光遗传学发展的重要事件[4]。在过去的几十年间,科学家开发了多种实验平台来标记或者控制神经元,但却一直没有很好的方法能同时在时间上和空间上实现对特定细胞的精确操纵——直到光感离子通道被开发出来,并在一代又一代的革新中投入应用。
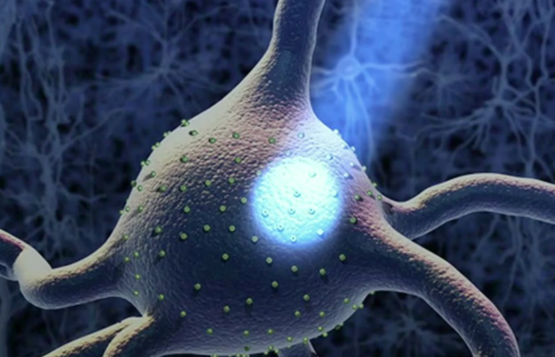 蓝色激光激活表达光感离子通道的神经元。图片来源:Liu Xu,Steve Ramirez
蓝色激光激活表达光感离子通道的神经元。图片来源:Liu Xu,Steve Ramirez
瞄准完成,激光命中目标
光感离子通道的特性就是在特定波长的光照刺激下,会专一地开放其通道,让特定的阳离子或者阴离子大量通过细胞膜,从而造成细胞膜两边的膜电位发生变化,最终造成该神经元选择性地兴奋或者抑制。
光感离子通道存在相当于新建了一条平行于该神经元固有活性外的新通路。研究者可以通过控制光的有无,来模拟特定神经元在接受特定刺激时的反应。刘旭等人选择的光感离子通道对蓝光敏感,因此只要给那些转基因小鼠头部做个小手术植入光纤,使光能直接照射到相应神经元,那么一旦光纤另一端给予蓝光脉冲,带有光敏感通道的神经元就会被模拟激活。
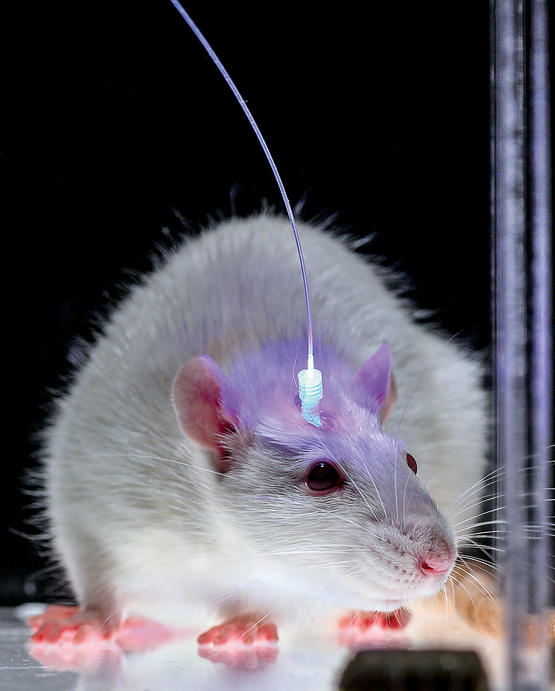 通过向转基因实验小鼠的大脑植入光纤,刘旭和同事利用光遗传学方法改变小鼠记忆。图片来源:Karl Deisseroth, John Carnett, Karl Deisseroth/sciencemag.org
通过向转基因实验小鼠的大脑植入光纤,刘旭和同事利用光遗传学方法改变小鼠记忆。图片来源:Karl Deisseroth, John Carnett, Karl Deisseroth/sciencemag.org
除了空间定位准确外,光遗传学方法在时间上也更加到位。如果用传统给药方法,从给药到药物发挥功能需要一定的时间,而且观察后期去除这些药物较为困难,而光刺激却可在几个毫秒内就打开光感离子通道,而在停止光刺激之后又能快速关闭光感离子通道。因此,虽然光遗传学的概念提出至今也就十来年,其应用却是非常广泛,现在,除了将光遗传学应用到精神疾病的机制研究外,科学家们还直接在小鼠模型里将光敏感蛋白表达在视网膜神经节细胞上,替代视网膜上退化的感光细胞,让疾病小鼠重见光明[5]。
用光创造虚假的记忆
技术平台搭建完成后,刘旭和同事接下来完成了整个实验设计中最巧妙的部分——标记对应某个特定记忆的细胞。他们以逸待劳,首先让这些负责特定记忆的细胞自我暴露,并且在暴露后全部都被标记,之后在需要操作它们的时候,用一束蓝色激光照射即可。
前面提到过那些转基因小鼠,平时一直喂食含有多西环素的鼠粮,此时没有光敏离子通道表达。准备开始给小鼠植入记忆时,他们首先停止喂食多西环素,打开了第一重开关,随后选择一个特定的刺激,比如轻微电击等,以使小鼠对恐惧相关的神经元激活,使只负责形成恐惧记忆的神经元的第二重开关也被打开。从此,这些神经元内光敏离子通道开始合成。通过这一精巧设计,小鼠脑中就有且只有负责恐惧记忆相关的神经元会表达光敏离子通道。在后续的实验中,只要通过激光开关控制再次激活这些光敏离子通道,就能重新模拟特定记忆了[6]。
 《科学》杂志2013年7月26日的封面,显示了刘旭及其合作伙伴改变小鼠记忆时小鼠大脑海马组织的免疫荧光图。图片来源:Xu Liu, Steve Ramirez /sciencemag.org
《科学》杂志2013年7月26日的封面,显示了刘旭及其合作伙伴改变小鼠记忆时小鼠大脑海马组织的免疫荧光图。图片来源:Xu Liu, Steve Ramirez /sciencemag.org
在之后的研究中,刘旭和同事设计各种不同的场景,并通过各种组合激活这些记忆,最终使得小鼠形成一个新记忆,但这个记忆的内容在现实中从未真正发生过,也就是一个虚假的记忆。整个精巧的实验设计一气呵成,令人叫绝[7]。
简单来说,就是将待测试转基因小鼠放在一个特定的环境A中,标记它记录有关环境A记忆的脑细胞。然后将小鼠放在一个完全不同的环境B中,唤起小鼠对环境A的记忆,同时给予小鼠轻微的电击,使小鼠错误地认为它是在环境A中受电击。刘旭等人发现,随后小鼠被放回环境A中时,尽管该环境从未有过电击危险,但由于这个虚假记忆的存在,它们还是而对环境A产生恐惧。
在同行类似课题的压力下,在历经无数次失败和摸索改进后,刘旭和同事这些耗费心力的工作,最终化作2012年和2013年在《自然》和《科学》上引起轰动的两篇论文。刘旭在接受采访时说:“我们的研究从实验上证明了人为改造记忆的可能性。这是第一次形成一个独立的虚假记忆。以前有过类似的研究,但无法产生一个探测得到的虚假记忆,而只是一个与真实记忆融合在一起,无法区分的混合记忆。”
刘旭的杰出工作在国内也引起了很好反响,2013年,复旦大学脑科学研究院请他回来进行学术交流——那应该是2002年出国之后,刘旭的第二次短期回国,趁此机会,我们生科院也邀请他回来看看,和同学们交流一下科研工作和感悟。我也终于有机会和刘旭进行深入交流。
那时,刘旭已在美国各高校开始了求职巡游。我曾侧面问他有没有回国的打算,对很多想过安稳日子的人来说,这是一个很不错的选择。但刘旭却有更高的目标。对他来说,科研和工作的本质更加纯粹,而国内的学术氛围还不能让他满意。虽然在美国,他可能只会有一个与国内相比非常小的实验室,所有事情都要亲历亲为,但他更乐意这样纯粹的科研环境。
那时,刘旭的科研引擎还在一刻不停地推动着更多结果的产出。2014年,他所在的实验室再一次在《自然》发表论文。在这篇论文中,他们深入研究了对记忆至关重要,却又不可相互取代的海马区(标记背侧齿状回,DG)和杏仁核(标记杏仁核基底外侧复合体,BLA)[8]。该项研究发现,通过将一种积极或消极记忆与多种刺激联系起来,可以改变与DG特定细胞群相联系的情绪,却不能改变与BLA特定细胞群相联系的情绪。这项惊人的神经科学研究结果,革新了更多人脑海中对“可能性”的定义。
2012年《自然》通过光遗传学方法激活记忆痕迹(memory engram)的研究,2013年《科学》操纵记忆痕迹细胞以产生虚假记忆的研究,以及2014年再度发表在《自然》通过记忆痕迹细胞改变记忆价(memory valence,定义为与某个记忆相联系的正面或负面的情绪)的研究论文,构成了完整的三部曲,使记忆痕迹理论深入到分子生物学层面。对脑科学感兴趣的果壳网友不妨读一下刘旭作为第一作者刚发表在《冷泉港定量生物学专题》的综述,该文在系统地介绍了记忆痕迹理论产生和发展的关键事件的基础上,以最通俗的方式介绍了他们操纵记忆三部曲的工作[9]。
壮志未酬
然而,正当越来越多的人为神经科学的新能力而惊叹的时候,那个曾向他们展示这种能力的人却永远地离去了。
不久前,刘旭才终于选定了他心目中理想的学校,位处芝加哥的西北大学。他在大雪中驱车千里赶到他在芝加哥的新家,愉悦地开始他独立PI的生涯,并憧憬在安定后,开始他幸福美满的家庭生活……谁也想不到,这富有希望的一切,竟以这样的方式戛然而止。
刘旭是不是已经在自己的脑海中设计好了进一步探索记忆奥秘的精巧实验?我们再也无法得知。但可以肯定的是,即便要花更多的时间和精力才能将那些设想变为现实,他的同行仍会将刘旭未竟的事业进行下去。很遗憾,我们再也无法听刘旭讲述他关于记忆的新故事,但他的工作,已为整个脑科学研究领域开拓了一片新的大陆。
刘旭与史蒂夫在TED大会的演讲。视频来源:ted.com
最后要谢谢各位被我骚扰并要求提出修改意见的各位好友,谢谢你们的中肯意见,希望此文能通俗易懂,激发更多的年轻人热爱科学。
(编辑:Calo)
参考文献:
- Lashley K. In search of the engram. Symp Soc Exp Biol (1950) 4: 454-82.
- Penfield W. Memory Mechanisms. AMA Archives of Neurology and Psychiatry (1952) 67: 178-198.
- Scoville WB and Milner B. Loss of recent memory after bilateral hippocampal lesions. J Neurol Neurosurg Psychiatry (1957) 20: 11-21.
- Liu X, and Tonegawa S. Optogenetics 3.0. Cell (2010) 141:22–24.
- Doroudchi MM, Greenberg KP, et, al. Virally delivered channelrhodopsin-2 safely and effectively restores visual function in multiple mouse models of blindness. Mol Ther (2011) 19: 1220-1229.
- Liu X, Ramirez S, Pang PT, Puyear CB, Govindarajan A, Deisseroth K and Tonegawa S. Optogenetic stimulation of a hippocampal engram activates fear memory. Nature (2012) 484: 381–385.
- Ramirez S, Liu X, Lin P, Suh J, Pignatelli M, Redondo RL, Ryan TJ, and Tonegawa S. Creating a false memory in the hippocampus. Science (2013) 341: 387–391.
- Redondo RL, Kim J, Arons AL, Ramirez S, Liu X, and Tonegawa S. Bidirectional switch of the valence associated with a hippocampal contextual memory engram. Nature (2014) 513: 426–430.
- Liu X, Ramirez S, Redondo RL, and Tonegawa S. Identification and manipulation of memory engram cells. Cold Spring Harb Symp Quant Biol (2015) doi: 10.1101/sqb.2014.79.024901.
