2015年诺贝尔化学奖得主之一,托马斯·林达尔(Tomas Lindahl)跟DNA打了近半个世纪的交道。这位原本的医学生在基础研究领域做出了一系列重要成果。他在探索DNA修复机制的过程中经历过什么?且看他亲自讲述:
 托马斯·林达尔和保罗·莫德里奇、阿齐兹·桑贾尔共享了今年的诺贝尔化学奖。图片来源:nobelprize.org
托马斯·林达尔和保罗·莫德里奇、阿齐兹·桑贾尔共享了今年的诺贝尔化学奖。图片来源:nobelprize.org
(果壳翻译班/编译)在我的研究生涯早期,大概1975或1976年吧,我从转染有EB病毒(人类疱疹病毒第四型)的伯基特淋巴瘤和鼻咽癌患者细胞中观察到,EB病毒的DNA出现了两种形态:除了整合到细菌DNA内部的片段之外,还出现了不被整合到宿主基因组的共价闭合环。这在当时十分令人惊讶,它比其他实验室后来在乳头瘤病毒上进行的类似研究都要早。
在20世纪70年代到80年代,我的一项主要研究成果,在于描述并量化了自发的内源性DNA损伤。令人惊讶的是,此过程中的主要事件,比如水解脱嘌呤、胞嘧啶残基脱氨基、鸟嘌呤和嘧啶残基的氧化以及腺嘌呤残基甲基化生成3-甲基腺嘌呤,总数量惊人——人体内每天会出现约10000个这样的潜在变异和细胞毒性变化。这些结果明确表明,一定存在特殊的DNA修复酶和机制,来抵消内源性DNA损伤。
我因此产生了了解DNA修复机制本质的热情。《自然》发表过一项综述文章,讨论内源性DNA损伤和它的修复。我发现了“碱基切除修复”的途径——这是内源性DNA损伤的主要细胞防线。后来,使用提纯蛋白,我们重构了碱基切除修复的两种变体:短补丁/长补丁。我发现了几种未曾为人所知的DNA修复酶作用模型,包括:(i)一种能催化碱基-糖键分裂的DNA糖基化酶(尿嘧啶-DNA糖基化酶)、3-甲基腺嘌呤DNA糖基化酶和释放氧化碱基残基的DNA糖基化酶。(ii)在无碱基的糖-磷酸残基上剪裁DNA双链的AP核酸内切酶(和沃尔特教授(Walter Verly)同时独立研究)。(iii)O6-甲基鸟嘌呤 - DNA甲基转移酶(MGMT,一种Ada蛋白:它能以不可逆的方式,从烷基化的DNA上,把一个促突变甲基基团,移到酶自己身上的一个特殊的半胱氨酸残基上)。(iv)DNA双加氧酶:(AlkB蛋白和它的同系物):它能从烷基化的碱基残基上移走某些有细胞毒性的甲基基团,办法是在铁和氧代戊二酸的存在下完成氧化脱甲基化的反应(和芭芭拉博士(Barbara Sedgwick)、俄林教授(Erling Seeberg)一起研究)。这种DNA修复机理也推动人们发现了几组新的酶——FTO和ALKBH5,它们可以对一种全新的表观遗传标记RNA m6A进行去甲基化。
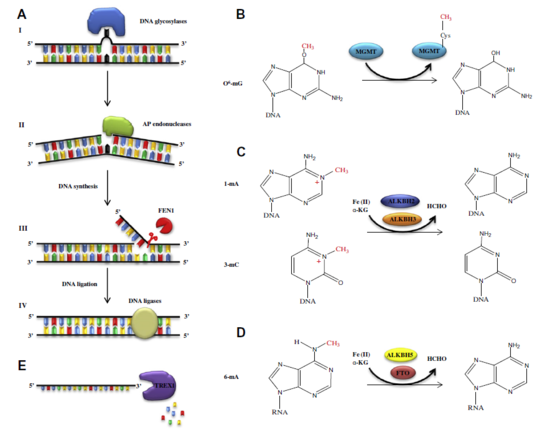 DNA修复的相关酶促反应机制模型。图片来源:Tomas Lindahl. Genomics, Proteomics & Bioinformatics, Volume 11, Issue 1, February 2013, Pages 2–7
DNA修复的相关酶促反应机制模型。图片来源:Tomas Lindahl. Genomics, Proteomics & Bioinformatics, Volume 11, Issue 1, February 2013, Pages 2–7
值得一提的是:我(与让•卡戴特教授合作)发现了一种复杂、并且化学性质稳定的DNA氧化损伤——环式嘌呤脱氧核糖核苷酸。与其他DNA氧化损伤不同,它的修复仅能由核苷酸切除修复完成。此外,我(与博士后研究员瑞克•伍德博士合作)建立起了不用人体细胞的依赖ATP的核苷酸切除修复系统。这个分析系统通过体外互补实验实现,它使纯化XPA(这一蛋白质在有修复缺陷的着色性干皮细胞中是缺失的)等蛋白质成为可能。
我对辨识和描述在真核细胞中的DNA连接酶是非常有兴趣的,它需要ATP而不是NAD作为辅基,这和大多数的细菌连接酶是有区别的。在哺乳动物的细胞中,主要的DNA连接酶包括:DNA连接酶I型(负责复制和修复),DNA连接酶III型(负责碱基切除修复),以及DNA连接酶IV型(负责非同类末端结合)。和Lee Johnston博士合作,DNA连接酶I型在1990年被克隆和测序,这让我们能够定位酶 - 腺苷酸复合物形成的活性位点。在此之前,人们观察到DNA连接酶I型在人类疾病中出现了变化,这些观测结果得到了部分的证实。
此外,我还发现并描述了哺乳动物细胞核内的两个主要的DNA特异性核酸外切酶,最开始被命名为DNase III和DNase IV,现在则分别被叫做TREX1和FEN1。FEN1是一种5-3核酸外切酶,这种复制和修复因子可以从DNA中剔除悬垂和翘起片段(该研究和迈克尔·利伯博士同期独立进行)。TREX1则是作用于DNA单链的3-5核酸外切酶。最近的研究表明,人体细胞如果失去TREX1会导致一种遗传性系统性红斑狼疮(SLE),被称作艾卡迪尔综合征(Aicardi-Goutières syndrome)(和雅尼克博士(Yanick Crow)共同完成)。2007年,我们发现单链DNA会在不含TREX1的细胞内积累,并造成持久的检查点激活(和同事杨运桂博士以及德伯拉博士(Deborah Barnes)共同完成)。
除发现了几个DNA修复酶之外,我也观察到了Ada蛋白的自甲基化,在调节域内甲基化了一个半胱氨酸残基。这是DNA磷酸三酯修复的结果,让Ada蛋白变成了一个转录因子。这项工作在1986年发表,是第一个转录后修饰事件能激活一个转录因子的实例。
除了我自己的科学研究之外,我也在管理许多实验室上花费了时间,并仍然对各家实验室各自的研究观念和方向上提供建议。作为帝国癌症研究基金会(ICRF)剑桥大学克莱尔学堂(Clare Hall)实验室和英国癌症研究院(Cancer Research UK)的前负责人,我很高兴看到克莱尔学堂实验室成为国际知名的研究DNA修饰的实验室。我也很高兴看到我很多前任同事在他们的学术领域获得了成功。
我仍然很享受做科学研究。它让人快乐,它有趣,它刺激。它一直在改变。我真希望能活到一百岁,看着科学如何发展。(编辑:Ent)
