上到帝王将相入海求仙的轶事,下至平民百姓不老嫦娥的神话,从古至今,人们从未停止追逐长生不老的梦。现代医学的进步延长了人类的寿命,但衰老依然总在发生。我们知道衰老可能带来什么,却仍不清楚到底是什么带来了衰老。DNA损伤的累积,活性氧的增多,端粒的缩短……一代代科学家从青年探索到垂暮,只为找到更多推动衰老发生的“元凶”。
前不久,美国加州索尔克研究所的胡安·巴尔蒙蒂(Juan Carlos Izpisua Belmonte)团队在对衰老机制的探索取得了惊人的成果——他们不但设法减轻了早衰症小鼠的衰老迹象,还成功延长这些小鼠的寿命。研究结果[1]发表在了《细胞》杂志上。
让衰老的细胞变“年轻”
每一个人类都由一个受精卵发育而来。在长达十个月的发育过程中,这颗受精卵会不断地分裂和分化,最终产生一个具有完整生理结构的个体。在相当长的一段时间内,科学家认为这样的过程是不可逆的,细胞仿佛只能遵循着某种编好的程序,经历从干细胞到已分化细胞的过程——具有全能性的受精卵可以转变成人们的皮肤、骨骼、神经、器官和毛发,但你却不能利用这些已经分化的组织再现一个具有分化潜能的细胞。
后来,日本科学家山中伸弥团队的研究颠覆了人们的认识:他们发现,在已分化细胞中诱导特定转录因子的表达,可以恢复这些细胞的多能性。也就是说,这些细胞可以被“重编程”回类似胚胎干细胞的状态[2]。山中伸弥因这一发现获得了诺贝尔奖,而那些能够用来产生干细胞的四种因子——Oct4,Sox2,Klf4,和c-Myc(OSKM),也被命名为“山中因子”(Yamanaka factor)。
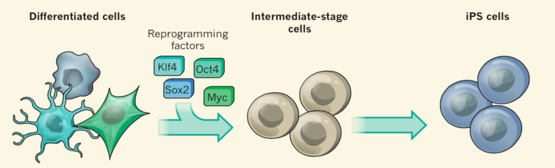 向已分化的细胞(Differentiated cells)里引入四种转录因子(Oct4,Sox2,Klf4和Myc),能够对细胞进行“重编程”,最终得到诱导性多功能干细胞(iPS cells)。诱导性多功能干细胞具有类似胚胎干细胞的能力,能够分化为多种不同类型的细胞。图片来源:参考文献[3]
向已分化的细胞(Differentiated cells)里引入四种转录因子(Oct4,Sox2,Klf4和Myc),能够对细胞进行“重编程”,最终得到诱导性多功能干细胞(iPS cells)。诱导性多功能干细胞具有类似胚胎干细胞的能力,能够分化为多种不同类型的细胞。图片来源:参考文献[3]
后来的研究表明,通过调控山中因子在细胞中的表达,人们能够对细胞进行不同程度的重编程。而在体外,细胞中那些与衰老相关的表现,也能够靠重编程来减轻[4]。这些发现给了巴尔蒙蒂灵感:用重编程回调已分化细胞的“年纪”可能促进组织再生,那么如果将类似的技术应用于体内,或许可以帮助我们人为地延缓整个生物个体的衰老。
为了验证自己的假设,巴尔蒙蒂选用了早衰症(Hutchinson-Gilford Progeria syndrome)的小鼠模型进行实验。患有早衰症的人类很早就会出现衰老症状,寿命往往只有十几岁。类似地,早衰症小鼠模型也会在幼年期就表现出衰老迹象,比如体重减轻和多种脏器的老化,寿命也会相应缩短。
巴尔蒙蒂的研究团队先从早衰小鼠身上分离出细胞做体外培养。借助基因工程,他们能够使用药物短时诱导“山中因子”表达,从而对这些细胞进行重编程。他们发现,相比于对照组细胞,经历重编程的细胞中与衰老相关的症状有了显著的改观。随后,他们又对年龄较大的野生型小鼠的细胞以及人类细胞进行相同的实验,得到了一致的结果。这证明,对细胞进行“重启”可能是逆转衰老的可行之道。
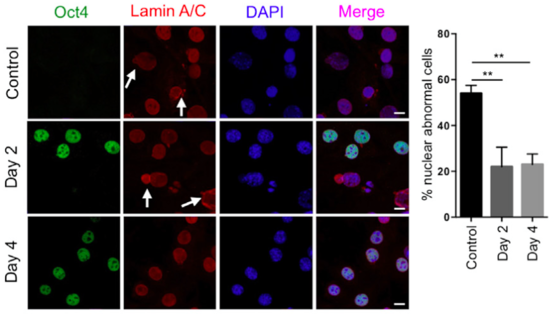 早衰症小鼠体内的Lmna基因发生突变,“早衰蛋白”(progerin)大量积累,促使小鼠过早地衰老。这些蛋白的积累会造成细胞核膜结构异常(起泡,如白色箭头所示),而在细胞中诱导表达山中因子(以Oct4为指标,绿色)2~4天能够显著减轻核膜异常的情况。图片来源:参考文献[1]
早衰症小鼠体内的Lmna基因发生突变,“早衰蛋白”(progerin)大量积累,促使小鼠过早地衰老。这些蛋白的积累会造成细胞核膜结构异常(起泡,如白色箭头所示),而在细胞中诱导表达山中因子(以Oct4为指标,绿色)2~4天能够显著减轻核膜异常的情况。图片来源:参考文献[1]
延长早衰小鼠的寿命
体外细胞实验的结果促使巴尔蒙蒂团队更进一步。他们希望利用相同的方法来让早衰的小鼠活得更长。但在实验的开始阶段,他们就遇到了一个麻烦:山中因子持续表达超过四天,早衰小鼠就呈现出高死亡率。这可能是因为对细胞进行部分重编程的过程中,器官中有大量细胞脱分化,导致很多重要的生理功能无法完成。为此,他们特别采用了循环诱导的方式——每次进行两天的连续诱导,然后停五天,如此反复。他们发现,经过这样处理的小鼠死亡率没有显著提升。通过调节山中因子的表达剂量,研究者也避免了肿瘤在小鼠体内形成。
研究发现,进行了“山中因子”表达治疗的小鼠,健康状况得到了很大程度的改善。相比于未受治疗的对照组,这些“返老还童”的小鼠在皮肤、肾脏、脾脏和胃等器官的健康状况都有了很大程度的改善。更为重要的是,它们对代谢类疾病和肌肉损伤的耐受度和恢复能力也更强。相比于未受治疗的其他早衰小鼠,它们的生理指标更接近健康鼠。这意味着,巴尔蒙蒂成功使这些本该垂垂老矣的小鼠变“年轻”了些。
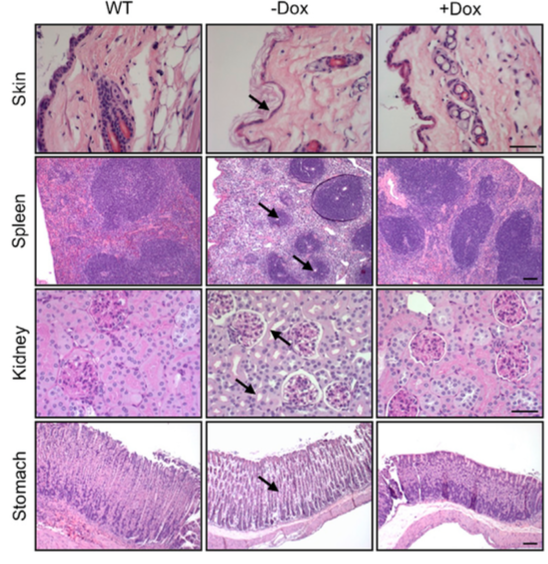 三个月大的不同小鼠的组织对比。一般的早衰小鼠(中列)在皮肤(Skin)中出现表皮变薄及角质化程度升高,在脾脏(Spleen)中出现较小的淋巴小结,在肾脏(S)中出现肾小管萎缩,在胃部则出现部分细胞损失(箭头所示)。这些症状在用药物诱导表达山中因子的早衰小鼠(右列)中都有减轻,组织的形态与同龄的野生型小鼠(左列)相对更接近。图片来源:参考文献[1]
三个月大的不同小鼠的组织对比。一般的早衰小鼠(中列)在皮肤(Skin)中出现表皮变薄及角质化程度升高,在脾脏(Spleen)中出现较小的淋巴小结,在肾脏(S)中出现肾小管萎缩,在胃部则出现部分细胞损失(箭头所示)。这些症状在用药物诱导表达山中因子的早衰小鼠(右列)中都有减轻,组织的形态与同龄的野生型小鼠(左列)相对更接近。图片来源:参考文献[1]
尽管这样的治疗并没能将早衰小鼠从体重不断减轻的命运中拯救过来,但却的确使得这些小鼠活得更长了。不做治疗的早衰小鼠,寿命的中位数只有区区18周;而接受治疗的早衰小鼠,这一数据被延长到了24周——最长寿的活到了接近30周。虽然和健康的野生型小鼠相比还有较大差距,但这样的结果已经令人惊喜。
不老梦要实现了吗?
巴尔蒙蒂的实验第一次证实了利用细胞重编程去“逆转”小鼠的时间轴是可行的。但值得注意的是,我们仍然远远没到声称人们完成了“返老还童”的时刻。毕竟目前的体内实验结果都还只是来自小鼠模型。
 16周大的早衰小鼠(左)、经山中因子表达治疗的早衰小鼠(中)和野生型小鼠(右)的状态对比。图片来源:参考文献[1]
16周大的早衰小鼠(左)、经山中因子表达治疗的早衰小鼠(中)和野生型小鼠(右)的状态对比。图片来源:参考文献[1]
事实上,直到今日,人们仍未找到“衰老”背后的确切原因。早在几年前,就有科学家发表研究成果,指出对端粒和线粒体基因组进行改造,能够一定程度上使得衰老的细胞“重焕青春”。巴尔蒙蒂等人在论文中指出,通过重编程来重置动物的衰老时钟,可能帮助我们更好地了解衰老背后的分子机制。只有最终弄清这一点,我们才可能想办法去更好地治疗与衰老有关的种种疾病,最终延长人的寿命。这项研究是人类追寻长寿梦想过程中的又一次伟大尝试,但要完成这一梦想,我们还需要更多的研究结果。
(编辑:Calo)
参考文献:
- Ocampo, Alejandro, et al. "In Vivo Amelioration of Age-Associated Hallmarks by Partial Reprogramming." Cell 167.7 (2016): 1719-1733.
- Takahashi, Kazutoshi, and Shinya Yamanaka. "Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors." Cell 126.4 (2006): 663-676.
- Loh, Kyle M., and Bing Lim. "Stem cells: Close encounters with full potential." Nature 502.7469 (2013): 41-42.
- Mahmoudi, Salah, and Anne Brunet. "Aging and reprogramming: a two-way street." Current opinion in cell biology 24.6 (2012): 744-756.
